中性粒细胞与肿瘤免疫
中性粒细胞是应对感染而出现的急性炎症细胞,由于其成熟后无法继续增殖,而且半衰期短(6-8小时),人们认为它只能在发挥特定的免疫功能,因此并未到得到过多关注。近年的研究发现,中性粒细胞不但拥有更长的存活时间,而且能够从损伤部位反向循环中迁移,在淋巴器官中可以促进T细胞的增殖和功能。结合中性粒细胞本身的功能特征,可能对肿瘤治疗有重要作用。
中性粒细胞发育
在骨髓中,多能粒细胞-单核细胞祖细胞(GMP)向中幼粒细胞发育的过程中,会经过eNeP、ProNeu2、PreNeu这几个阶段,它们能够增殖并且每个阶段有独特的基因表达特征。有人认为,在肿瘤中这几种的亚型会产生不同的细胞群,与肿瘤的发生发展相关。
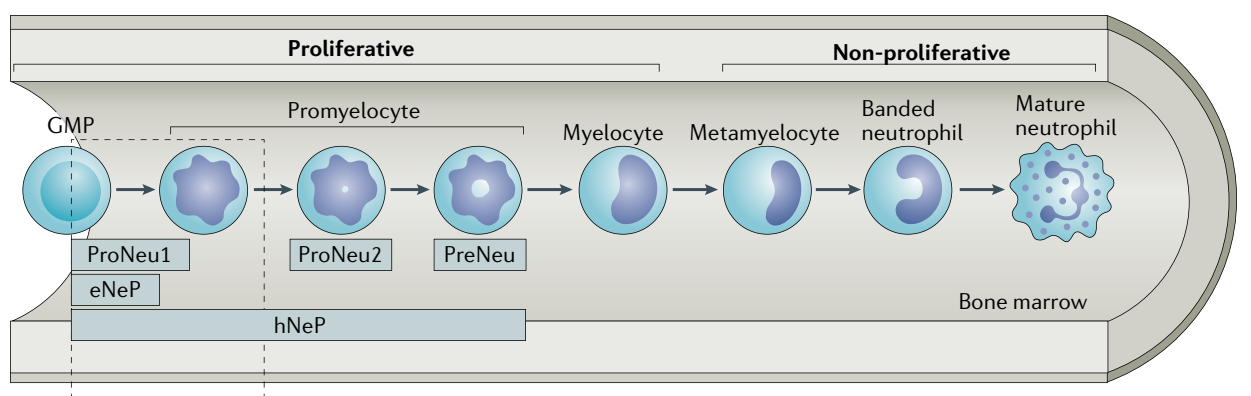
eNep/ProNeu:早期中性粒细胞祖细胞; PreNeu:中性粒细胞前体
Nat Rev Immunol. 2022
未成熟的中性粒细胞能够从骨髓中被直接释放,在外周随着衰老而产生不同的表型和功能。而且骨髓外成熟的中性粒细胞也具有异质性,通过CyTOF分析,肿瘤患者体内存在至少7种成熟的中性粒细胞亚群。这些异质性中性粒细胞的发现,为我们了解其在肿瘤中的作用以及制定治疗方法中发挥重要作用。
中性粒细胞与肿瘤
促瘤作用
肿瘤的发生与祖细胞增殖和功能增强的致癌性突变、肿瘤前炎性环境的建立有关。中性粒细胞在炎症反应中重要地位自然在肿瘤发生过程中有重要意义,它通过以下方式,促进肿瘤发生。
- 暴露于致癌物时,中性粒细胞通过产生ROS,加重DNA氧化损伤,促进肿瘤发生。
- 在TME中,中性粒细胞功能受到干扰,表现出高度重塑。肿瘤相关中性粒细胞(TANs)通过释放中性粒细胞外陷阱(NET)增强肿瘤细胞的增殖。
- 中性粒细胞诱导锌指蛋白SHAI1的表达,通过缺氧促进肿瘤细胞上皮间充质转化(EMT),而且SHAI1会继续促进中性粒细胞的募集。
- 通过促进血管新生。
- 肿瘤细胞中NOTCH1的激活,使中性粒细胞响应TGF-β信号而发挥免疫抑制作用。并且细胞上还会表达PD-L1。
- 释放的NET能够保护肿瘤细胞免遭CTL的毒性杀伤。
- 促进肿瘤炎症发生、γδT细胞活化。
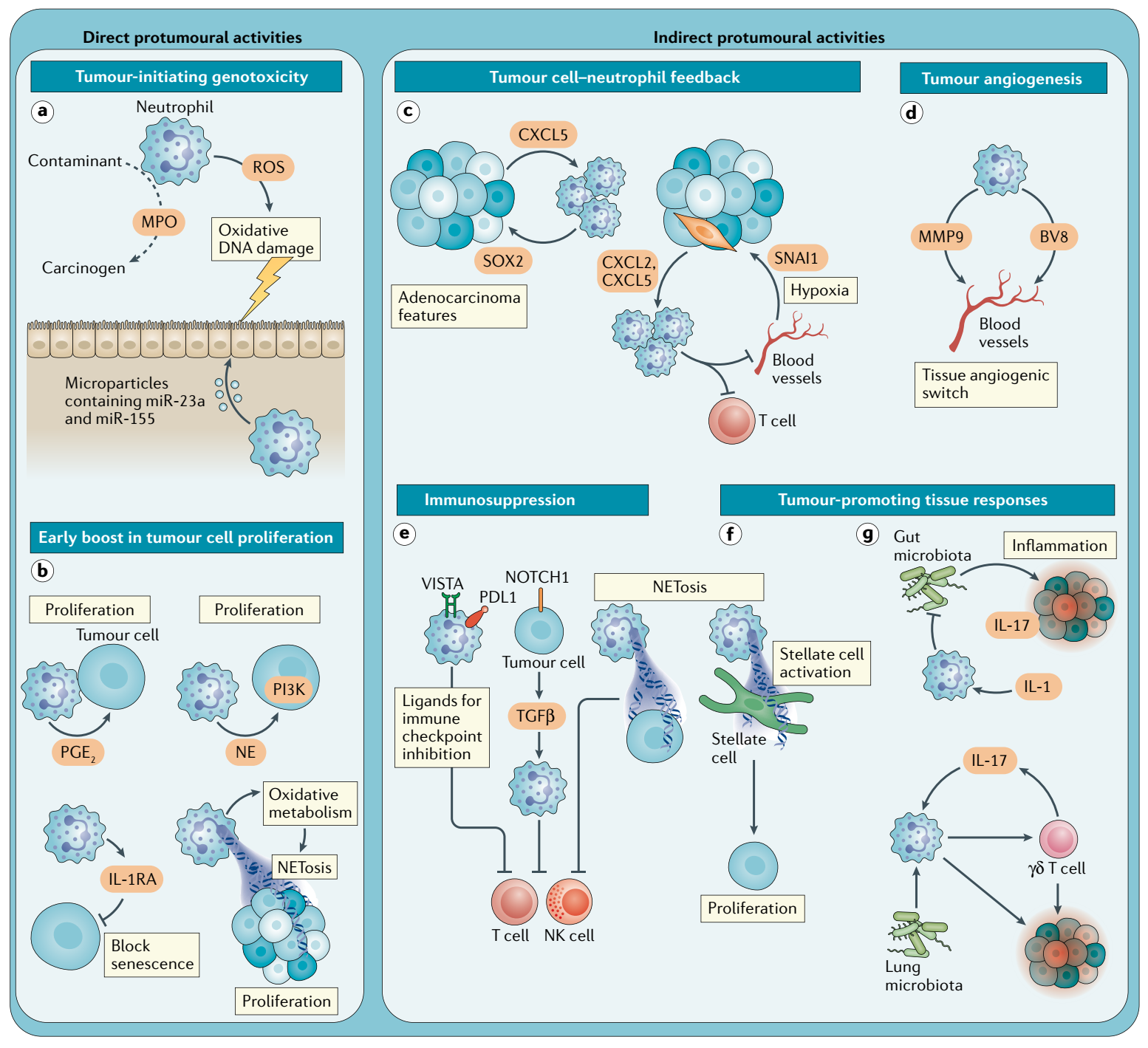
Nat Rev Immunol. 2022
同时,中性粒细胞能够通过以下方式,促进肿瘤转移。
- 与肿瘤细胞结合成簇,支持肿瘤细胞周期进展。
- 中性粒细胞代谢改变,通过氧化磷酸化和上调脂肪酸转运蛋白2(FATP2),促进免疫抑制和肿瘤生长
- 肿瘤衍生外泌体会激活肺部上皮细胞中Toll样受体3(TLR3),进而促进免疫抑制性中性粒细胞募集。
- 肺部间充质细胞促进中性粒细胞的脂质积累,并由中性粒细胞将脂质转移到肿瘤细胞中,促进肿瘤增殖。
- 诱导细胞外基质(ECM)重塑。
- 肿瘤细胞上NET相关DNA(CCDC25)的特定传感器通过激活整合连锁激酶(LIK)信号促进肿瘤转移。
- 暴露在脂多糖环境中,会触发NET介导的ECM重塑,并唤醒休眠的肿瘤细胞。脂多糖募集的中性粒细胞也会降低血小板反应蛋白1促进肿瘤转移。
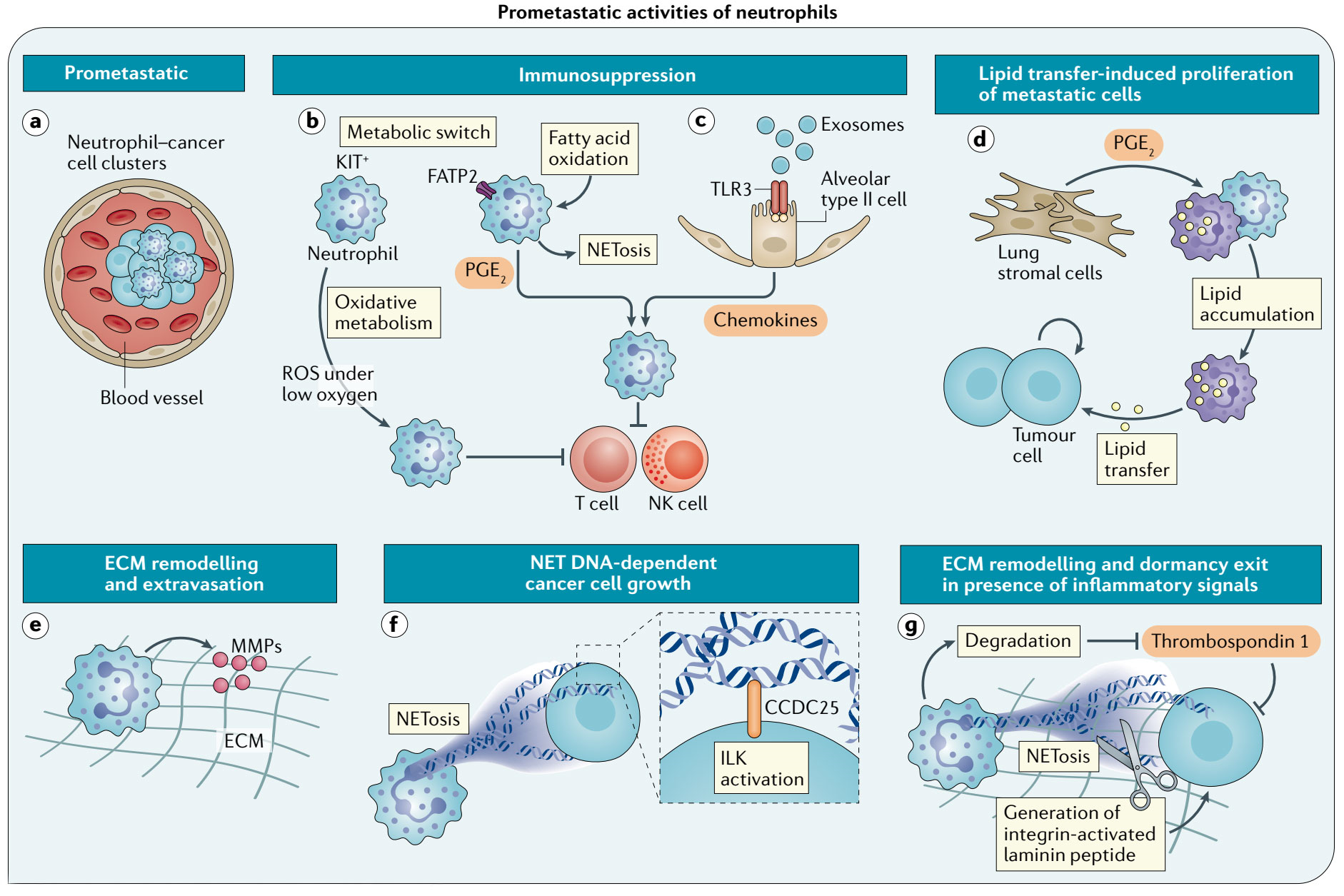
Nat Rev Immunol. 2022
抗瘤作用
中性粒细胞在肿瘤中并非只有消极的一面,在抑制肿瘤生长和转移方面也具有一定作用。
- 中性粒细胞能够诱导肿瘤从基底层脱离,阻止肿瘤生长。
- 释放NO杀死肿瘤细胞。
- 通过Fc介导的质膜摄取杀伤肿瘤。
- 增加TME中INFγ量,使巨噬细胞分泌IL-12,促进αβT细胞的肿瘤抑制作用。
- 与APC杂交融合,从而增强T细胞的肿瘤抑制作用。
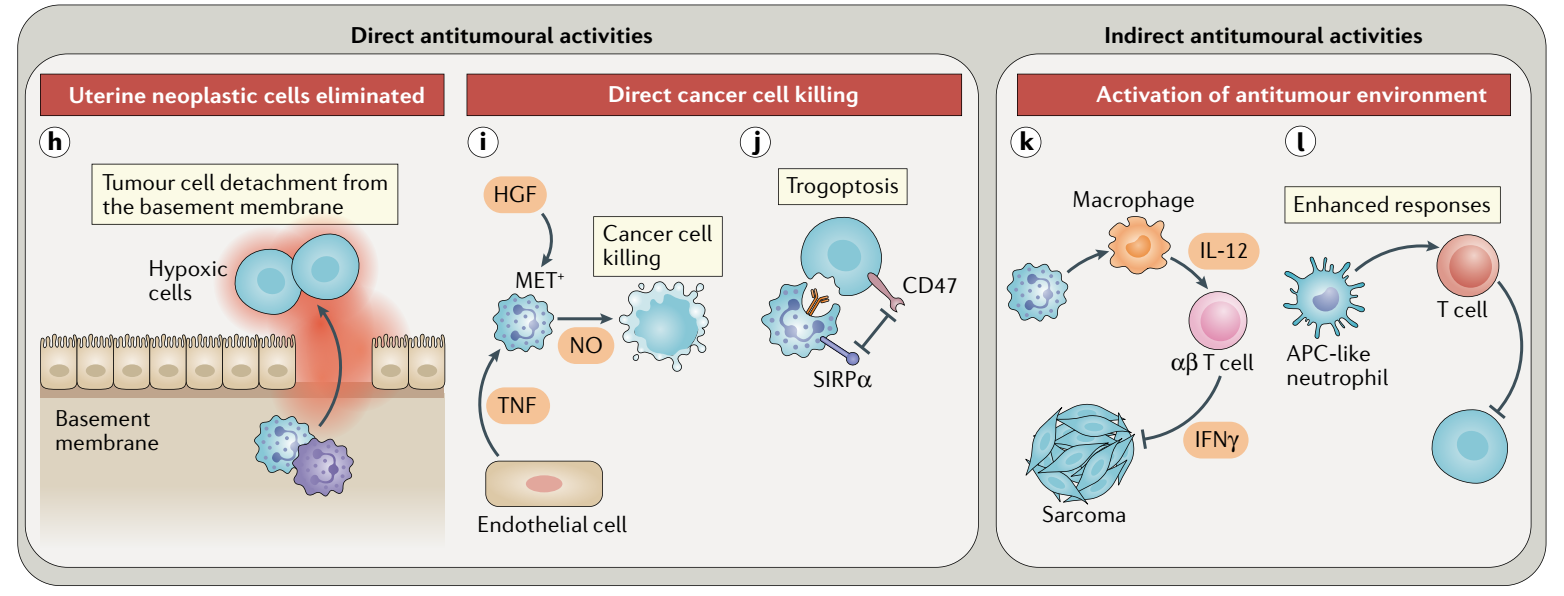
Nat Rev Immunol. 2022
- 维持上皮间充质转变(EMT),抑制肿瘤转移的启动。
- 聚集在转移前部位的中性粒细胞通过H2O2杀死浸润的肿瘤细胞。
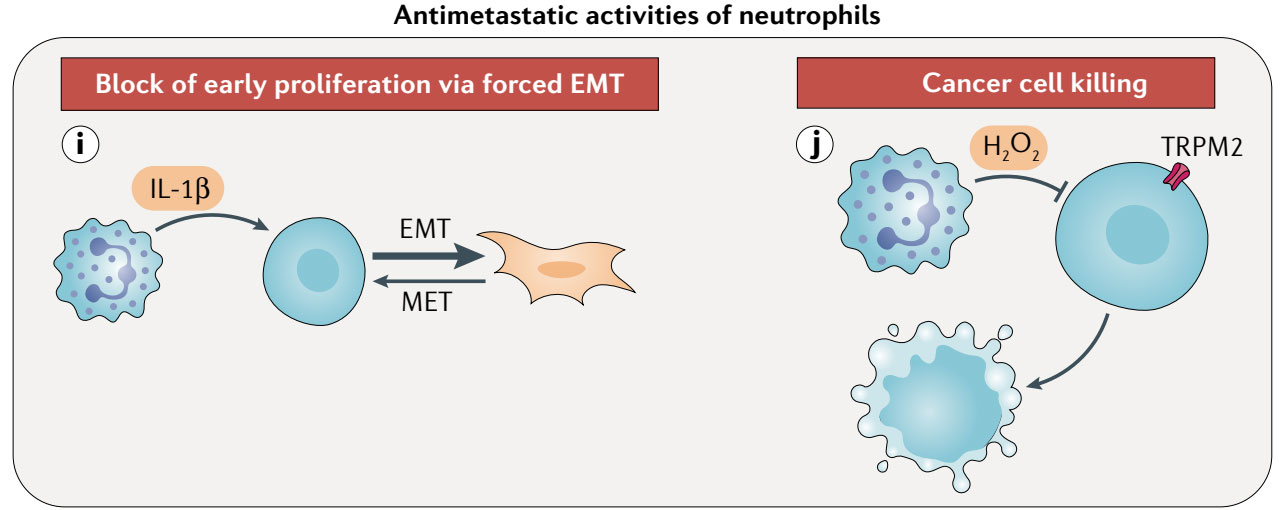
Nat Rev Immunol. 2022
小结
中性粒细胞在肿瘤中的表现提示它具有一定的治疗开发价值,然而它的本身的特性也为开发带来了技术上的难题,短期很难成为主流的治疗手段。
但鉴于它对环境的适应性和肿瘤中的异质性,目前可作为制定治疗策略的参考依据,或对疗效进行预测的工具。
参考资料
- Wculek SK et al. Early Neutrophil Responses to Chemical Carcinogenesis Shape Long-Term Lung Cancer Susceptibility. iScience. 2020 Jul 24;23(7):101277.
- Cristinziano L et al. . Anaplastic Thyroid Cancer Cells Induce the Release of Mitochondrial Extracellular DNA Traps by Viable Neutrophils. J Immunol. 2020 Mar 1;204(5):1362-1372.
- Szczerba BM et al. Neutrophils escort circulating tumour cells to enable cell cycle progression. Nature. 2019 Feb;566(7745):553-557.
- Yang L et al.. DNA of neutrophil extracellular traps promotes cancer metastasis via CCDC25. Nature. 2020 Jul;583(7814):133-138.
- Gershkovitz M et al.. TRPM2 Mediates Neutrophil Killing of Disseminated Tumor Cells. Cancer Res. 2018 May 15;78(10):2680-2690.